再生医療研究に 新たな価値をもたらす スキャフォールド素材の登場

コラーゲン、フィブロネクチン、ラミニン、ビトロネクチンなど、細胞外マトリックス由来のスキャフォールド試薬が各社から出る中、富士フイルム株式会社(以下、富士フイルム)から新たなコンセプトのスキャフォールド試薬「cellnest(セルネスト)ヒトⅠ型コラーゲン様リコンビナントペプチド」(以下 セルネスト)が発売された。同製品の開発に初期の頃から関わる、同社執行役員R&D統括本部再生医療研究所所長の吉岡康弘氏と、現在開発の中心を担う中村健太郎氏に話をうかがった。そこから、この製品が研究者のアイデア次第で用途の多様性を広げられるポテンシャルを持った、単なるスキャフォールド用途にとどまらない、ひと味違った素材であることがみえてきた。
カラーフイルム技術が生み出した新素材
カラーフイルム断面の電子顕微鏡像と光学顕微鏡像を前に、「フイルムは化学プラント」と熱弁する吉岡氏が説明する同社のフイルムのケミストリーは、鮮明なカラー写真を追求する中で築き上げてきた技術の高さを実感させる。たった約20µmの厚みしかないフイルム感光層の限られた空間に、ナノテクノロジーと材料研究の粋を結集した機能を持った層が10以上重なる。そこには、同社が近年注力する医薬、化粧品、再生医療につながる、特徴的な三つの要素が活かされている。一つ目は、独自のナノテクノロジー。粒子の分散度を飛躍的にあげる技術とノウハウを武器に、リポソーム内への親水性分子の封入技術など、DDSの新しい境地を拓きつつある。二つ目の、カラーフイルムの色あせの原因である活性酸素による酸化を防ぐ技術は、すでに化粧品で活用され、市場展開が進む。そして三つ目が、写真フイルムの主原料であるコラーゲンの高機能化、高品質化に長年挑戦し続ける中で蓄積された膨大な知見と、その特性を活かすために培ってきた技術だ。こうしたナノテクノロジー、ケミストリーの独自技術基盤も持ちながら、コラーゲン材料の開発ができるという、他社にはない研究開発環境から生まれてきたのが、「cellnest(セルネスト)ヒトⅠ型コラーゲン様リコンビナントペプチド」だ。
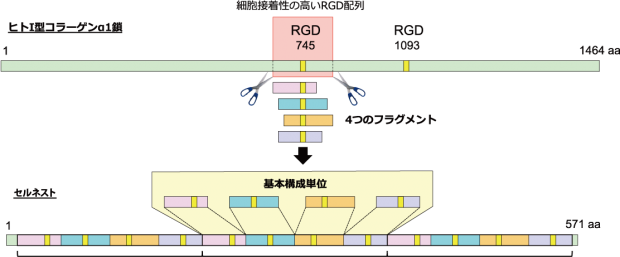
図1 セルネストの構造
抗原性の低いヒトI型コラーゲンα1鎖から切り出した、4つの細胞接着性の高いRGD配列を含むフラグメントを1つの基本構成単位としている。これを3つタンデムにつなげた、12個のRGD配列を持つリコンビナントペプチドがセルネストだ。
細胞接着の共通アミノ酸モチーフに注目したセルネスト
すでに多くのメーカーから動物由来成分を含まないスキャフォールド試薬が出ている中で、セルネストの新しさは何か。大きく分けると、細胞接着の機序に着目した分子構造、動物由来成分を含まずかつGMPグレードの高い品質、そして多様な加工に対応できる素材としての汎用性の高さが挙げられる。
セルネストは、コラーゲンをはじめ、ラミニン、フィブロネクチンなどの細胞外マトリックスの受容体として機能するインテグリンの認識配列を人工的につなぎ合わせたリコンビナントペプチド(以下、RCP)だ。コラーゲンで最も一般的なI型コラーゲンを構成するポリペプチド鎖の中で、抗原性の低いα1鎖からインテグリンが認識するRGD(アルギニン-グリシン-アスパラギン酸)配列を含むフラグメントを4つ選び出し、12個のリピートができるように並べた構造をとる(図1)。「インテグリンのαVを抗体でブロックしたときにRGDと細胞の接着が起こらないことを実験で確認する中で、RGDがインテグリンを介して結合していることを確信していきました」と開発に携わってきた中村氏は振り返る。これまでに接着細胞での事例を積み重ねており、例えばHUVECを用いた細胞接着性の評価では、高い細胞接着性が確認されている(図2)。
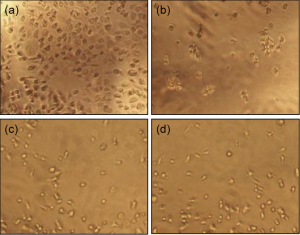
図2 各種スキャフォールド素材を用いたときのHUVECの播種試験結果
0.2µg/wellとなるように、セルネスト (a) 、市販リコンビナントゼラチン (b)、牛ゼラチン(pI5)(c)、豚ゼラチン(pI9)(d)、でシャーレをコートし、HUVECを播種すると、セルネストが最も高い細胞接着性を示した。
再生医療現場で使える製品仕様
二つ目の特徴である、動物由来成分を含まずかつGMPグレードの高い品質については、臨床まで一気通貫で見据える同社の姿勢が現れる。「研究用途だけで終わるのではなく、再生医療で使うことを意識して、本当に人で使用できるようにGMP基準の施設において製造しています。研究成果を患者さんに利用したいという意志を持っている研究者には、ぜひ利用してもらいたい」と吉岡氏は強調する。子会社のFUJIFILM Diosynth Biotechnologiesが持つGMP対応の生産設備で、バイオ医薬品生産で実績がある発現用酵母を使い、動物由来成分を含まない条件のもとでRCPの生産が始まっている。
高い加工性でさらに広がるポテンシャル
加工が容易なベプチド材料と捉えると、セルネストの可能性はさらに広がる。物性としては数十%の濃度で溶液に溶かすことができ、低温にするとゲル化し、温度を上げると再び溶解するというゼラチンに近い性質を併せ持つ。さらに架橋度合いは変えられるため、用途にあわせた形にできる。スポンジ、フィルム、ビーズ、ハイドロゲルなどに加工して、再生医療分野での用途開発が進行中だ。例えば、スポンジにしたRCPを骨欠損したマウスに移植した実験では、RCPが分解されながら、骨再生が促進される結果が得られている(図3)。「RCP自体にはサイトカインのような分化誘導を促進する機能はありませんが、分化誘導を促進する刺激が与えられた条件下では、その刺激をうまく拾い上げて、分化をさらに促進させる効果があることがわかってきています」という中村氏の説明は、再生医療での新たな用途を感じさせてくれる。
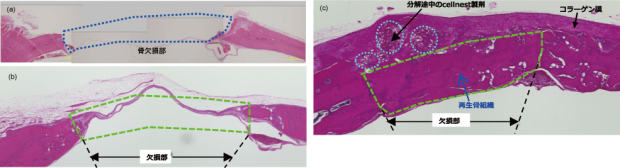
図3 ラット頭蓋骨欠損モデルにおける骨再生評価
ラットの頭蓋に欠損部を作り(a)、セルネスト製スポンジの移植の有無で8週間経過を観察したときの結果。セルネスト製スポンジを移植した場合(c)は、移植無しの場合(b)と比べて既存の骨に近い良好な骨の再生が認められた。
枠にとらわれない利用方法を提供するセルネストは、一度手に取って自分のアイデアを試してみるだけの価値を十分に持っている。
製品に関するお問合せはこちら
富士フイルム株式会社 再生医療事業推進室(担当者:上野)
- [ 所在地 ] 東京都港区赤坂9-7-3
- [ TEL ]03–6271–3030
- [ E-mail ][email protected]

