バイオ医薬研究を加速する、ベンチトップのシングルユースバイオリアクター

ここ数年、バイオ医薬品の研究や製造といった場面で、哺乳動物細胞を用いたタンパク質生産の需要が高まってきている。また再生医療の実用化に向けても、細胞の大量調製を実現する浮遊培養法への期待は大きい。そのような背景の中、より安全、確実かつ効率的な培養が可能なバイオリアクターの登場が有望視されている。今回、これまでの要望に応えることをコンセプトに開発され、さらに撹拌方法を工夫することで、よりパフォーマンスの向上が期待きる、2〜20Lスケールのシングルユースバイオリアクター ポールXRS 20を紹介する。
需要が高まるシングルユースバイオリアクター
昨今、国内の研究戦略の動向として実用化を目指したプロジェクト型予算がつくことが多く、今後アカデミアの中でも実証試験としてリットルオーダーの培養を行うシーンが出てくるのではないかと考えられる。特にタンパク質製剤の生産が目的の場合、翻訳後修飾を考慮すると、大腸菌や酵母でなく哺乳動物細胞が選択されるだろう。また、初期コストや、洗浄により発生する手間やコンタミリスク、ダウンタイムの低減などを目的として、従来のステンレスやガラス製タンクを備えた装置に加え、プラスチックバッグを用いるシングルユース技術の採用が活発化している。こうした背景を元に、各社から製品化されているのが哺乳類動物細胞培養用のシングルユースバイオリアクターだ。シングルユース培養バッグには、培地やフィード添加ポート、ガス供給ポートなどが備えられている。そのバッグのデザインや通気方法、培養パラメータの制御方法、撹拌方法等によって、各社の製品に違いが生まれている。
様々な企業から哺乳動物細胞用のシングルユースバイオリアクターが販売されている中、製品選択にあたって重要視されるのが、安全面や使いやすさの面に加え、培養・生産の効率や、細胞へのストレスだろう。これらに影響を与える要素として、撹拌の方法とそれに伴う培地の均一化までに要する時間、せん断力等によるストレス、溶液内での物質移動速度などが挙げられる。XRS 20が独自性を示すのが、独立二軸のモーターによる撹拌だ(図1)。混合のされやすさ、細胞にかかる負荷の低減を狙ったこの機構により、細胞培養に重要な複数の指標において、一軸モーターでシーソーのように揺らすバイオリアクターと比較して優位なデータが示されているのだ。
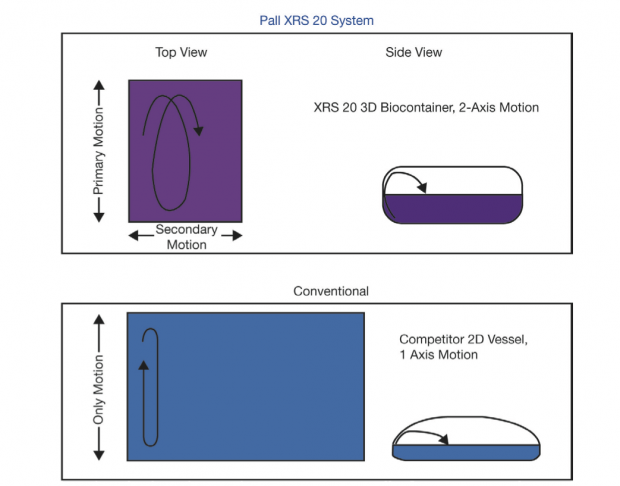
図1 XRS 20 (上)と従来のシーソー型バイオリアクター(下)との撹拌方式の違い。 XRS 20では二軸モーターにより渦を描くように培地が動き撹拌効率が高いが、シーソー型では横方向への移動速度が遅くなる。
XRS 20が示す撹拌効率、培養・生産の優位性
バイオリアクターの性能を見る際、重要な観点のひとつが、培養系の均一化にかかる時間の短さだろう。これを確認するため、20Lの模擬培地を使用した撹拌試験が実施された。pHを7.0±0.1で安定化させた後、4MNaOHを添加してpH約8.0で平衡化されるまでの時間が計測された結果、XRS 20では16秒で全体が平衡化されたのに対し、シーソー型のものではバッグの端にNaOHを添加してから中心部が平衡化するまでに50秒、バッグ全体が平衡化するまでに98秒を要した(XRS 20の約6倍)。これは、二軸モーターによる撹拌では培地が渦を描くようにバッグ全体を巡るため、より効率的に撹拌されていることを示すものである。
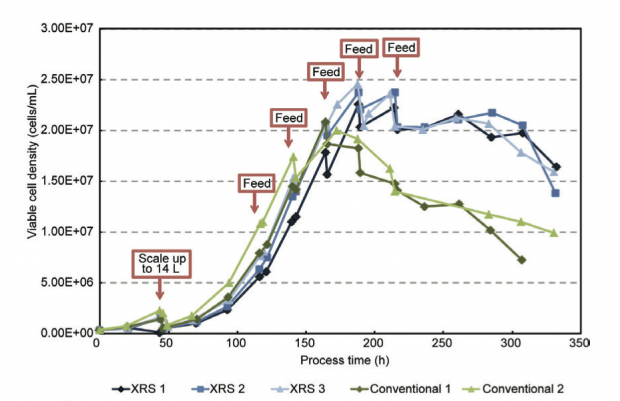
図2 CHO細胞培養時の生細胞数。いずれの方式でも培地量5Lで開始し、3.0 ± 1.0 × 106 cells/mLに達した後に培地を加え 14 Lにスケールアップした。その後、8.0 ± 2.0 × 106 cells/mLに達した際にEfficient Feed C(Life Technologies)を 1.2 L加え、さらに24時間おきに4回添加して、最終量を 20 Lにした。
さらに、モノクローナル抗体を産生するCHO細胞を培養した際に示したデータを見ていこう。まず細胞の増殖効率を示したのが図2だ。シーソー型のものだと、培養開始後170時間程度で生細胞数は約2×107cells/mLに達した後、徐々に低下していった。それに対してXRS 20では、約190時間後にピークを迎えた後、100時間程度は高い細胞数を維持できている。また抗体産生量(力価)は、シーソー型(N=2)の平均を100%として、XRS 20(N=3)では150%以上を示した(図3)。さらに、抗体の品質(チャージバリアント、修飾糖鎖)については、XRS 20とシーソー型のものとの間で差は見られなかった。つまり、XRS 20での培養は、シーソー型と比較し、高い生細胞数を長時間維持するだけでなく、同等の品質の抗体を約1.5倍の量を産生したことが分かる。
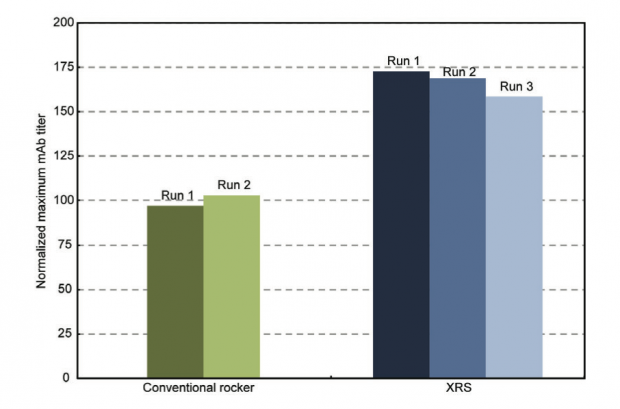
図3 CHO細胞が生産した抗体量を、培地の力価で示した。シーソー型(N=2)の平均を100%として計算。
医薬生産や再生医療で望まれる、低ストレス浮遊培養
近年、抗体医薬やタンパク質製剤に加え、再生医療の産業化推進により、細胞培養の自動化、大容量化のニーズが高まっている。ロボットアームを用いた接着細胞の自動培養システム構築といったアプローチがある一方で、コストを下げ培養の空間密度を上げる意味で、浮遊培養系への期待は大きい。しかし、特にES細胞やiPS細胞の培養においては、浮遊培養の際に撹拌による細胞にかかるせん断力等のストレスにより分化誘導がかかる(1)など、課題はまだ多い。また、浮遊培養で産業化が進むCHO細胞でも、せん断力をかけるとタンパク質の生産量が低下し、0.80N・m-2の場合49%にまで下がるという報告もあるのだ(2)。
XRS 20によりこれらの課題を解消できると考える日本ポール株式会社およびPall Corporationは、培養の際に細胞にかかるストレスの定量化や、より効率的な培養方法を探索するためのパートナーシップを組める研究者を求めている。また、現状は細胞をバッグ内に残したままの培地交換方法には開発の余地が見られ、再生医療目的で細胞を培養するには検討が必要だが、この面での開発も進められている。バイオ医薬産業の発展に伴って、多様なシーンでの使用が見込まれるベンチトップ型のシングルユースバイオリアクターの今後に期待したい。
【参考文献】
1) Chen KG. et al. Human pluripotent stem cell culture: considerations for maintenance, expansion, and therapeutics. Cell Stem Cell (2014), 14(1), 13-26
2) Keane JT. et al. Effect of shear stress on expression of a recombinant protein by Chinese hamster ovary cells. Biotechnol Bioeng. (2003), 81(2), 211-20.
【お問い合わせ先】
●日本ポール株式会社
[ 所在地 ] 東京都新宿区西新宿6–5–1
[ T E L ]03–6386–0995
[ E- mail ][email protected]
[ U R L ]https://www.pall.com/jp/ja.html
*日本ポール株式会社では、第27回リバネス研究費Pall XRS 20バイオリアクター賞にてXRS 20を用いた研究テーマを募集しています。(2015年6月30日締切)
